
分子スケールWG
多剤排出トランスポーターの機能を粗視化分子シミュレーションで実証
京都大学理学研究科
(左から)高田 彰二、姚 新秋、検崎 博生

ほとんどの薬が効かなくなる多剤耐性は、院内感染やがん化学治療などで重大な社会問題を引き起こしています。この多剤耐性化にはいくつかの異なる機構があります。
院内感染で大きな問題となった緑膿菌の場合は、細菌膜に存在するRND型などの多剤排出トランスポーターの発現量が増え、抗生物質を菌外に排出してしまうことが主な原因となっています。
RND型の多剤排出トランスポーターは、細胞内外の酸性度(pH)の違いを利用してH+(プロトン)が移動することによって駆動され、その力を利用して薬剤を排出します。
大腸菌由来のRND型多剤排出トランスポーター「AcrB」の原子構造は、2002年および2006年に村上聡氏(現、東工大教授)らがX線結晶構造解析を使って解明しました。
2002年の構造解析では、AcrBは、同じ分子が3つ集合した3回対称性をもつ3量体をとることが明らかになり、2006年の構造解析では、それぞれの分子が膜のプロトン輸送と薬剤排出の機能をもち、AcrB3量体は非対称な構造をしていることが分かりました。
非対称なAcrB3量体構造の1つ目の分子では細胞内に向いた薬剤の入り口と思われる経路が開き(取込型)、2つ目の分子では薬剤が中央に結合し(結合型)、3つ目の分子では細胞外に向いた薬剤排出口が開いていた(排出型)。
村上らは、AcrB3量体の3つの分子がこの3つの機能状態を順に経由することで薬剤を排出していると考えました。
3つの分子が各々の状態を一段階変えていくごとに、構造全体ではちょうど120度回転したように見えることから、この薬剤排出のメカニズムを「機能的回転機構」と名付けました。
しかし実験系による検証実験が難しく、この仮説の実証はできていませんでした。
私たちは文部科学省の「次世代生命体統合シミュレーションソフトウエアの研究開発」プロジェクトの一環で、生体分子の粗視化分子シミュレーション技法の開発を独自に進めてきました。
本研究では、この新しい技法を適用して、多剤排出トランスポーターAcrBのゆらぎに起因する機能シミュレーションを行いました。
(1)AcrB3量体の機能的回転と薬剤排出:非対称なAcrB3量体構造のうち、薬剤が結合しているAcrB分子(図1左の青)に細胞外からプロトンが結合すると、薬剤が外側に排出され(図1中央)、それと前後して、ほかの2つのAcrB分子も状態を変化させて機能的回転が起こりました(図1右)。
これによりプロトン結合をきっかけに機能的回転が起こり、薬剤排出が生じうることが示されました。
(2)AcrB3量体の休止状態:非対称なAcrB3量体構造から薬剤を取り除くと、3回対称性をもつ構造が安定になることが分かりました。 この構造は2002年の構造に近いものです。 すなわち2006年の構造解析で得た構造はAcrB3量体が薬剤を排出している途中のスナップショットで、2002年の構造は薬剤がないときの休止状態にそれぞれ対応していると考えられます。
参考文献
Xin-Qiu Yao, Hiroo Kenzaki, Satoshi Murakami & Shoji Takada, Drug
export and allosteric coupling in a multidrug transporter revealed by molecular
simulations" Nature Communications. 1, 117 (8 pages) (2010)
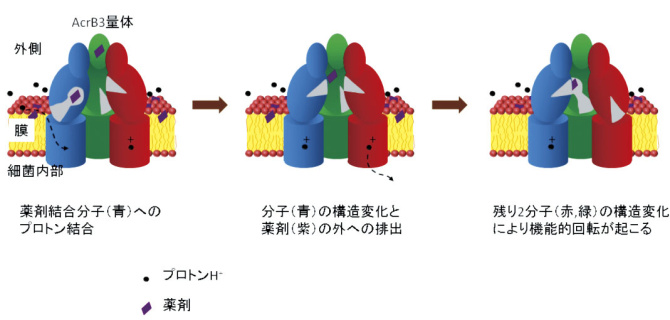
図1:プロトン結合によるAcrBの薬剤排出と機能的回転 |
BioSupercomputing Newsletter Vol.4
- SPECIAL INTERVIEW
- 経験重視の観察型医療から予測型医療への転換を図り、理論医学の基盤を構築するために
東海大学医学部内科学系(循環器内科)教授
東海大学医学研究科バイオ研究医療センター代謝疾患研究センター長
東海大学総合医学研究所代謝システム医学部門長 後藤 信哉 - シミュレーション科学の活用で栄養学や健康管理の新たな可能性が拓かれることに期待
味の素株式会社 ヘルスインフォマティクス班
グループ・エクゼクティブ・プロフェッショナル員 安東 敏彦
- 研究報告
- 多剤排出トランスポーターの機能を粗視化分子シミュレーションで実証(分子スケールWG)
京都大学理学研究科 高田 彰二/姚 新秋/検崎 博生 - 時空間を考慮した細胞シミュレーション(細胞スケールWG)
理化学研究所 次世代計算科学研究開発プログラム 須永泰弘 - 強力集束超音波による低侵襲治療のためのHIFUシミュレータの開発(臓器全身スケールWG)
理化学研究所 VCADシステム研究プログラム 沖田 浩平 - 大規模数理モデル構築を目的とした共有モデル開発プラットフォーム:PLATO(脳神経系WG)
①理化学研究所 次世代計算科学研究開発プログラム
②理化学研究所 脳科学総合研究センター
稲垣 圭一郎 ①/観音 隆幸 ②/ Nilton L. Kamiji ②/槇村 浩司 ②/臼井 支朗 ①②
- 報告
- BMB2010(第33回日本分子生物学会年会 第83回日本生化学会大会、合同大会)におけるワークショップ開催報告
- 生命体統合シミュレーション ウィンタースクール2011
理化学研究所 次世代計算科学研究開発プログラム 石峯 康浩(臓器全身スケールWG)
東京大学医科学研究所 浦久保 秀俊(脳神経系WG)
理化学研究所 次世代計算科学研究開発プログラム 須永 泰弘(細胞スケールWG)
理化学研究所 次世代計算科学研究開発プログラム 舛本 現(開発・高度化T)
理化学研究所 次世代計算科学研究開発プログラム 三沢 計治(データ解析WG)
理化学研究所 次世代計算科学研究開発プログラム 宮下 尚之(分子スケールWG)
