
分子スケールWG
細胞レベルの精緻な代謝モデルを用いた
肝臓シミュレータの開発と実証に向けて

慶應義塾大学医学部
谷内江 綾子
肝臓の大部分を占める肝実質細胞(肝細胞)は、生体で起こる代謝反応のほぼ全てを包含する非常に広範で複雑な代謝経路を持ち、生体内のあらゆる低分子の調節において重要な役割を果たしています。その機能の切り替えを効率的にしているのが、類洞血流の上流(門脈)側と下流(中心静脈)側で酵素の発現量が異なる、部位特異性を利用した代謝の区画化であると考えられています。しかし、肝細胞内では、多くの代謝機能は互いに深く関連しており、状況によって速度や制御機構が巧みに切り替わる肝代謝を包括的に理解するのは非常に難しく、多くの現象が状況証拠からの類推に留まっています。このような場合、シミュレーションによる動的特性の解析は非常に大きな力を持ちます。
そこで、文献検索による反応速度論情報に基づいて、約500個の定義物質、約250反応数に及ぶ、これまでに類を見ない大規模な代謝シミュレーションモデルをE-Cellシミュレーションソフトウェア注釈1上に組み上げました。このモデルでは、ミトコンドリアと細胞質で起こる代謝を同時に計算することができ(細胞内での代謝区画化の考慮)、酵素量を変えて門脈型、中心静脈型の特性を持たせたうえで、ギャップ結合を介した両細胞の低分子交換の影響をシミュレーションすることができます(細胞間での代謝区画化の考慮)。更に、Riken Cell Simulator(RICS)注釈2を用いることで、代謝特性の異なる肝細胞が互いに連結して機能している状態を再現しました(図1)。
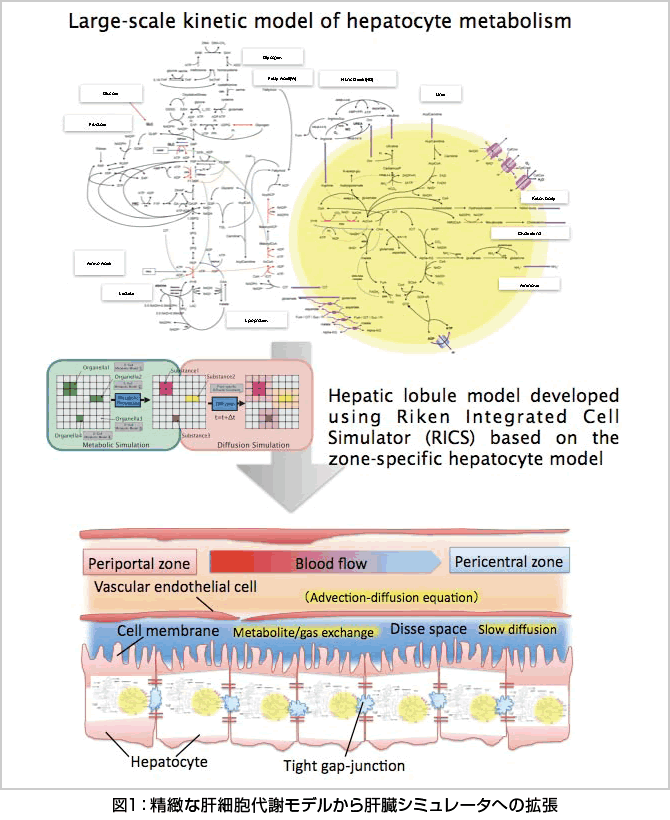
門脈型と中心静脈型の代謝特性を持つ2つの肝細胞が連結している場合と、門脈型のみ、中心静脈型のみの場合を設定して低酸素、低血糖状態のシミュレーションを行いました。その結果、特性の異なる細胞同士がカップリングすることで、これらの刺激に対する代謝物の変動、ATPエネルギーの低下が小さく抑えられ、臓器全体の代謝のロバストネスが向上していることが予測されました。
この結果は、肝代謝がheterogeneityを利用してどのように最適化されているかを理解する一助になるだけでなく、肝硬変による細胞間物質交換の障害における代謝不全の理解にも役立つと考えています。また、大腸がんの肝転移によって、転移病巣はもちろんのこと、その周辺の肝細胞においても代謝が大きく変動していることが当研究室の実験から明らかになってきました。我々の肝臓代謝シミュレーションモデルは、こういった病態モデルの再現と考察、手術中の肝虚血耐性や肝切除時の予備能の予測に応用することができます。
一方で、細胞の代謝が臓器、生体全体に与える影響、そのなかでも特に病態を考える際には、組織の構造を壊さずに代謝の状態を観察する実験系が必須になってきます。
そこで、我々の教室では、メタボローム解析と質量顕微鏡注釈3を組み合わせる事で、数ミリメートル間隔の領域を1ピクセルとする「代謝の可視化」の実験技術の開発を進めています(Hattori K et al., AntioxidRedox Signal. 13(8):1157-67 (2010))。 現在、本手法の改良が急ピッチで進んでおり、アミノ酸を含むより多くの代謝物をより高解像度で計測できるようになってきました。この技術により、門脈型と中心静脈型の肝細胞における代謝の差異を、vivoでの形状を維持したまま計測、定量することが可能になります(図2)。
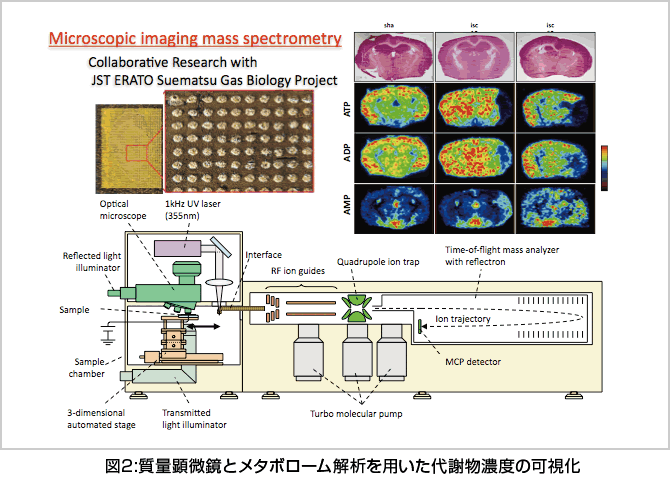
今後は、組織の三次元構造をそのままに代謝を定量、観察し、その結果や物質変動の意味を空間や位置を考慮した精緻な細胞シミュレーション(スパコンによる大規模な計算)によって解き明かす研究が重要になると考えています。
注釈1:慶應義塾大学先端生命研究所と理化学研究所が開発している、細胞内の生命現象に特化したシミュレーション環境。
注釈2:理化学研究所で開発されている、細胞シミュレーションの共通基盤。固定格子の空間(ボクセル)内に細胞のモデルを構築してボクセル間の拡散、移動などを設定することで、細胞内の場や細胞間の位置を考慮した生命現象をシミュレーションできます。
注釈3: 凍結組織の切片に微細な間隔でレーザーを当てて代謝物をイオン化し、繋がれている質量分析計で測定後、それぞれの位置に各測定代謝物の質量の情報を再構築することで、10マイクロメートルの解像度で質量分布を可視化します。
BioSupercomputing Newsletter Vol.3
- SPECIAL INTERVIEW
- さまざまな最先端研究基盤を統合して活かすためにも
スーパーコンピュータの果たす役割は大きい
持田製薬株式会社 医薬開発本部 専任主事 東北大学 客員教授 西島 和三 - 超音波治療の推進および治療機器開発に欠かせない生体の音響的シミュレーション研究
東京大学大学院 工学系研究科 機械工学専攻 特任研究員 佐々木 明
- 研究報告
- QM/MD/CGMのマルチスケール分子シミュレーションの実現(分子スケールWG)
大阪大学蛋白質研究所 米澤康滋/山中秀介/下山紘充/山﨑秀樹/中村春木
理化学研究所 次世代計算科学研究開発プログラム 福田育夫 - 細胞レベルの精緻な代謝モデルを用いた
肝臓シミュレータの開発と実証に向けて(細胞スケールWG)
慶應義塾大学医学部 谷内江 綾子 - MEGADOCKによる網羅的タンパク質間相互作用予測(データ解析融合WG)
東京工業大学大学院情報理工学研究科 秋山 泰/松崎 由理/内古閑 伸之/大上 雅史 - 昆虫嗅覚系全脳シミュレーション(脳神経系WG)
東京大学先端科学技術研究センター 加沢 知毅
- 報告
- 生命体統合シミュレーションサマースクール2010を開催
理化学研究所次世代計算科学研究開発プログラム 石峯 康浩(臓器全身スケールWG)
東京大学医科学研究所 島村 徹平(データ解析WG)
理化学研究所次世代計算科学研究開発プログラム 須永 泰弘(細胞スケールWG)
京都大学大学院情報学研究科 本田 直樹(脳神経系WG)
理化学研究所次世代計算科学研究開発プログラム 舛本 現(開発・高度化T)
理化学研究所次世代計算科学研究開発プログラム 松永 康佑(分子スケールWG) - 生命体統合シミュレーション・サマースクール2010へ参加して
東京大学大学院理学系研究科博士課程1年 齊藤 健
